Материаловедение
решение заданий по материаловедению
Зависимость скорости коррозии от рН
pH среды. pH равно отрицательному логарифму концентрации ионов водорода: pH=-lg[H']. При рН=7 среда нейтральная, рН7 - щелочная. Стойкость металла в среде с данным pH определяется растворимостью продуктов его коррозии, защищающих поверхность металла от дальнейшей коррозии. По зависимости скорости коррозии К от pH среды металлы делят на пять групп (рисунок 1). Диаграмма (а) характерна для благородных металлов (Au, Pt), для которых скорость коррозии мала и не зависит от pH. Диаграмма (б) характерна для Fe, Сu - малостойких в кислых средах и устойчивых в щелочных. Диаграмма (в) характерна для Al, Sn, Zn - устойчивых в нейтральных средах и сильно корродирующих в кислых и щелочных. Диаграмма (г) характерна для Ni, Сr - малостойких в кислых средах, умеренно стойких в нейтральных и стойких в щелочных. Диаграмма (д) характерна для W, Мо - малостойких в щелочных средах, умеренно стойких в нейтральных и стойких в кислых
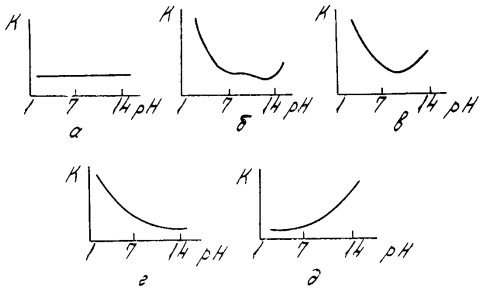
Рис. 1 – Виды зависимостей скорости коррозии от рН среды
 |
На нашем сайте Вы можете заказать решениe заданий по всем разделам материаловедения. |