Материаловедение
решение заданий по материаловедению
Виды двойных сплавов
В сплавах в зависимости от природы сплавляемых компонентов и характера их физико-химического взаимодействия могут образовываться различные но строению и свойствам продукты. Характер взаимодействия компонентов при сплавлении зависит от их положения в Периодической таблице Д. И. Менделеева, особенностей строения электронных оболочек их атомов, типов и параметров их кристаллических решеток, соотношения их температур плавления и других факторов. В зависимости от преобладания тех или иных факторов компоненты при сплавлении могут образовывать смеси зерен (с пренебрежимо ничтожной взаимной растворимостью), растворы (с неограниченной или ограниченной растворимостью друг в друге), химические соединения.
Особенность смесей заключается в том, что они состоят из зерен обоих компонентов, сохраняющих присущие им типы кристаллических решеток и физико-механические свойства.
Твердые растворы образуются при растворении компонентов друг в друге. Образующийся при этом твердый раствор состоит из зерен, кристаллическая решетка которых построена из атомов обоих компонентов. Различают твердые растворы замещения и твердые растворы внедрения. Если атомы растворимого компонента замещают в узлах кристаллической решетки атомы компонента-растворителя, то образующийся раствор называют твердым раствором замещения (рис. 2.1, а). Такие растворы образуют компоненты с аналогичным типом кристаллических решеток при небольшом отличии их параметров.
Если радиус атома растворимого элемента значительно меньше радиуса атома растворителя, то образуется твердый раствор внедрения (рис. 2.1, б). При образовании твердого раствора внедрения энергозатраты оказываются меньшими, так как атомы растворимого компонента не вытесняют атомы растворителя из узлов кристаллической решетки, а располагаются в междоузлии ячейки решетки.
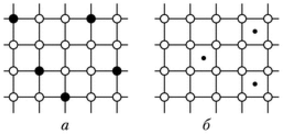
Рис. 2.1 Твердые растворы замещения (а) и внедрения (б)
Твердые растворы замещения могут быть ограниченными и неограниченными, а твердые растворы внедрения могут быть только ограниченными. При неограниченной растворимости атомы сплавляемых компонентов способны размещать в узлах кристаллической решетки при любом количественном соотношении. Это возможно при условии, если компоненты имеют одинаковый тип кристаллических решеток и их атомные радиусы отличаются не более чем на 8%. Неограниченную растворимость имеют, например, сплавы меди с золотом, германия с кремнием и др.
При ограниченной растворимости, когда способность компонентов растворяться друг в друге исчерпывается, образуются или смеси зерен ограниченных твердых растворов обоих компонентов друг в друге, или смеси зерен ограниченного раствора и химического соединения компонентов.
В твердых растворах замещения основной связью между атомами является металлическая. В твердых растворах внедрения наряду с металлической может возникать и ковалентная связь. Твердые растворы внедрения образуются при сплавлении переходных металлов с неметаллами, имеющими малый атомный радиус. Примером твердого раствора внедрения является твердый раствор углерода в железе. В зависимости от модификации железа растворимость углерода резко различается. Так. максимальная растворимость углерода в гамма-железе с ГЦК-решеткой составляет 2.14% (по массе), а в альфа-железе с ОЦК-решеткой-0,02%.
При растворении углерода в ОЦК-решетке альфа-железа каждый атом углерода отдает два валентных электрона на образование металлической связи, а два других - на образование ковалентных направленных трехцентровых (Fe-С-Fe) связей с двумя ближайшими атомами железа. Ковалентная связь на порядок сильнее металлической, что отражается на увеличении прочностных свойств сплава.
В твердых растворах внедрения искажение кристаллической решетки больше, чем в твердых растворах замещения. Более того, в твердых растворах внедрения при увеличении концентрации растворенного элемента существенно возрастают твердость, прочность, но вместе с тем снижаются пластичность, электропроводность.
Химические соединения, образующиеся по правилу валентности при сплавлении двух компонентов, имеют строго определенный состав. Им свойственна специфическая кристаллическая решетка, отличающаяся от решеток обоих компонентов. Ячейки решеток химических соединений имеют сложное строение, а связь между атомами в них сильнее и жестче металлической. Свойства химического соединения резко отличаются от свойств образующих его компонентов.
Соединения металла с неметаллами (нитриды, карбиды и др.) относятся к обычным химическим соединениям, хотя они частично могут обладать металлической связью. Многие химические соединения. образующиеся в металлических сплавах, не подчиняются закону валентности и не имеют постоянного состава. Соединения одних металлов с другими называют интерметаллическими или интерметаллидами. В таких соединения преобладает металлическая связь, и они не подчиняются закону валентности, например Fe2Mo, Ni3Ti, Ni3AI и др.
В химических соединениях сохраняется простое кратное соотношение компонентов. Если компоненты обозначить буквами А и В. то состав химического соединения выражают формулой AmBn где m и n — простые числа.
Химические соединения обычно образуются между компонентами, имеющими значительные различия в кристаллических решетках и в электронном строении атомов. Если образующиеся в сплавах химические соединения оказываются стойкими веществами, не диссоциирующими при нагреве вплоть до температуры плавления. то их рассматривают как самостоятельные компоненты, способные образовывать сплавы с другими компонентами данного сплава. Примером химического соединения, имеющего важное практическое значение для железоуглеродистых сплавов, является карбид железа Fe3C, о котором будет подробно сказано в гл. 5.
Особенность смесей заключается в том, что они состоят из зерен обоих компонентов, сохраняющих присущие им типы кристаллических решеток и физико-механические свойства.
Твердые растворы образуются при растворении компонентов друг в друге. Образующийся при этом твердый раствор состоит из зерен, кристаллическая решетка которых построена из атомов обоих компонентов. Различают твердые растворы замещения и твердые растворы внедрения. Если атомы растворимого компонента замещают в узлах кристаллической решетки атомы компонента-растворителя, то образующийся раствор называют твердым раствором замещения (рис. 2.1, а). Такие растворы образуют компоненты с аналогичным типом кристаллических решеток при небольшом отличии их параметров.
Если радиус атома растворимого элемента значительно меньше радиуса атома растворителя, то образуется твердый раствор внедрения (рис. 2.1, б). При образовании твердого раствора внедрения энергозатраты оказываются меньшими, так как атомы растворимого компонента не вытесняют атомы растворителя из узлов кристаллической решетки, а располагаются в междоузлии ячейки решетки.

Рис. 2.1 Твердые растворы замещения (а) и внедрения (б)
Твердые растворы замещения могут быть ограниченными и неограниченными, а твердые растворы внедрения могут быть только ограниченными. При неограниченной растворимости атомы сплавляемых компонентов способны размещать в узлах кристаллической решетки при любом количественном соотношении. Это возможно при условии, если компоненты имеют одинаковый тип кристаллических решеток и их атомные радиусы отличаются не более чем на 8%. Неограниченную растворимость имеют, например, сплавы меди с золотом, германия с кремнием и др.
При ограниченной растворимости, когда способность компонентов растворяться друг в друге исчерпывается, образуются или смеси зерен ограниченных твердых растворов обоих компонентов друг в друге, или смеси зерен ограниченного раствора и химического соединения компонентов.
В твердых растворах замещения основной связью между атомами является металлическая. В твердых растворах внедрения наряду с металлической может возникать и ковалентная связь. Твердые растворы внедрения образуются при сплавлении переходных металлов с неметаллами, имеющими малый атомный радиус. Примером твердого раствора внедрения является твердый раствор углерода в железе. В зависимости от модификации железа растворимость углерода резко различается. Так. максимальная растворимость углерода в гамма-железе с ГЦК-решеткой составляет 2.14% (по массе), а в альфа-железе с ОЦК-решеткой-0,02%.
При растворении углерода в ОЦК-решетке альфа-железа каждый атом углерода отдает два валентных электрона на образование металлической связи, а два других - на образование ковалентных направленных трехцентровых (Fe-С-Fe) связей с двумя ближайшими атомами железа. Ковалентная связь на порядок сильнее металлической, что отражается на увеличении прочностных свойств сплава.
В твердых растворах внедрения искажение кристаллической решетки больше, чем в твердых растворах замещения. Более того, в твердых растворах внедрения при увеличении концентрации растворенного элемента существенно возрастают твердость, прочность, но вместе с тем снижаются пластичность, электропроводность.
Химические соединения, образующиеся по правилу валентности при сплавлении двух компонентов, имеют строго определенный состав. Им свойственна специфическая кристаллическая решетка, отличающаяся от решеток обоих компонентов. Ячейки решеток химических соединений имеют сложное строение, а связь между атомами в них сильнее и жестче металлической. Свойства химического соединения резко отличаются от свойств образующих его компонентов.
Соединения металла с неметаллами (нитриды, карбиды и др.) относятся к обычным химическим соединениям, хотя они частично могут обладать металлической связью. Многие химические соединения. образующиеся в металлических сплавах, не подчиняются закону валентности и не имеют постоянного состава. Соединения одних металлов с другими называют интерметаллическими или интерметаллидами. В таких соединения преобладает металлическая связь, и они не подчиняются закону валентности, например Fe2Mo, Ni3Ti, Ni3AI и др.
В химических соединениях сохраняется простое кратное соотношение компонентов. Если компоненты обозначить буквами А и В. то состав химического соединения выражают формулой AmBn где m и n — простые числа.
Химические соединения обычно образуются между компонентами, имеющими значительные различия в кристаллических решетках и в электронном строении атомов. Если образующиеся в сплавах химические соединения оказываются стойкими веществами, не диссоциирующими при нагреве вплоть до температуры плавления. то их рассматривают как самостоятельные компоненты, способные образовывать сплавы с другими компонентами данного сплава. Примером химического соединения, имеющего важное практическое значение для железоуглеродистых сплавов, является карбид железа Fe3C, о котором будет подробно сказано в гл. 5.