Материаловедение
Поляризация и деполяризация при коррозии
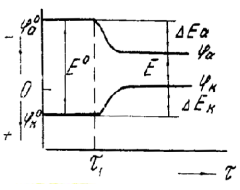
Рисунок 1 - схема изменения потенциалов катода и анода после замыкания цепи
Причиной поляризации является торможение (маленькая скорость) одной или нескольких составляющих процесса электрохимической коррозии. В результате скорость накопления отрицательных зарядов на аноде или положительных на катоде становится меньше скорости перехода электронов от анода к катоду и потенциалы анода и катода изменяются. Поскольку скорость всего процесса определяется скоростью самой медленной (лимитирующей) стадией, то в результате поляризации скорость коррозии в целом замедляется. Анодная поляризации (торможение анодного процесса) может быть вызвана медленным выходом ионов металла в раствор (лимитирует химическая реакция), образованием на поверхности металла защитной оксидной пленки или медленным отводом ионов металла от поверхности, что затрудняет выход следующих (лимитирует диффузия). Катодная поляризации (торможение катодного процесса) может быть вызвана маленькой скоростью окисления катионов или молекул раствора на поверхности металла (лимитирует химическая реакция) или медленным подводом кат ионов или молекул раст вора к поверхности катода и отводом продукгов восстановления от катода в раствор (лимитирует диффузия).
Деполяризацией называются явления, способствующие увеличению скорости коррозионных процессов и соответственно уменьшению поляризации электродов. Вещесгва, уменьшающие поляризацию называются деполяризаторами. Наиболее распространенными катодными деполяризаторами являются водород и кислород - основные окислители в растворах. Коррозия с участием ионов водорода возможна в случае, когда равновесный потенциал металла отрицательнее равновесного потенциала водородного электрода в данных условиях. Деполяризующее действие будет оказывать увеличение содержания в растворе водорода. Коррозия с участием молекул кислорода - наиболее распространенный случай. Деполяризующее действие будет оказывать увеличение содержания в растворе кислорода. Деполяризующее действие будут также оказывать растворение защитной оксидной пленки и все факторы, облегчающие доступ окислителей к поверхности металла, например, перемешивание.
 |
На нашем сайте Вы можете заказать решениe заданий по всем разделам материаловедения. |